Anvisa aprova segundo lote da vacina CoronaVac
Diferença da análise do segundo lote para o primeiro está no fato de que o envase e os processos de rotulagem e embalagem ocorrem no Instituto Butantan
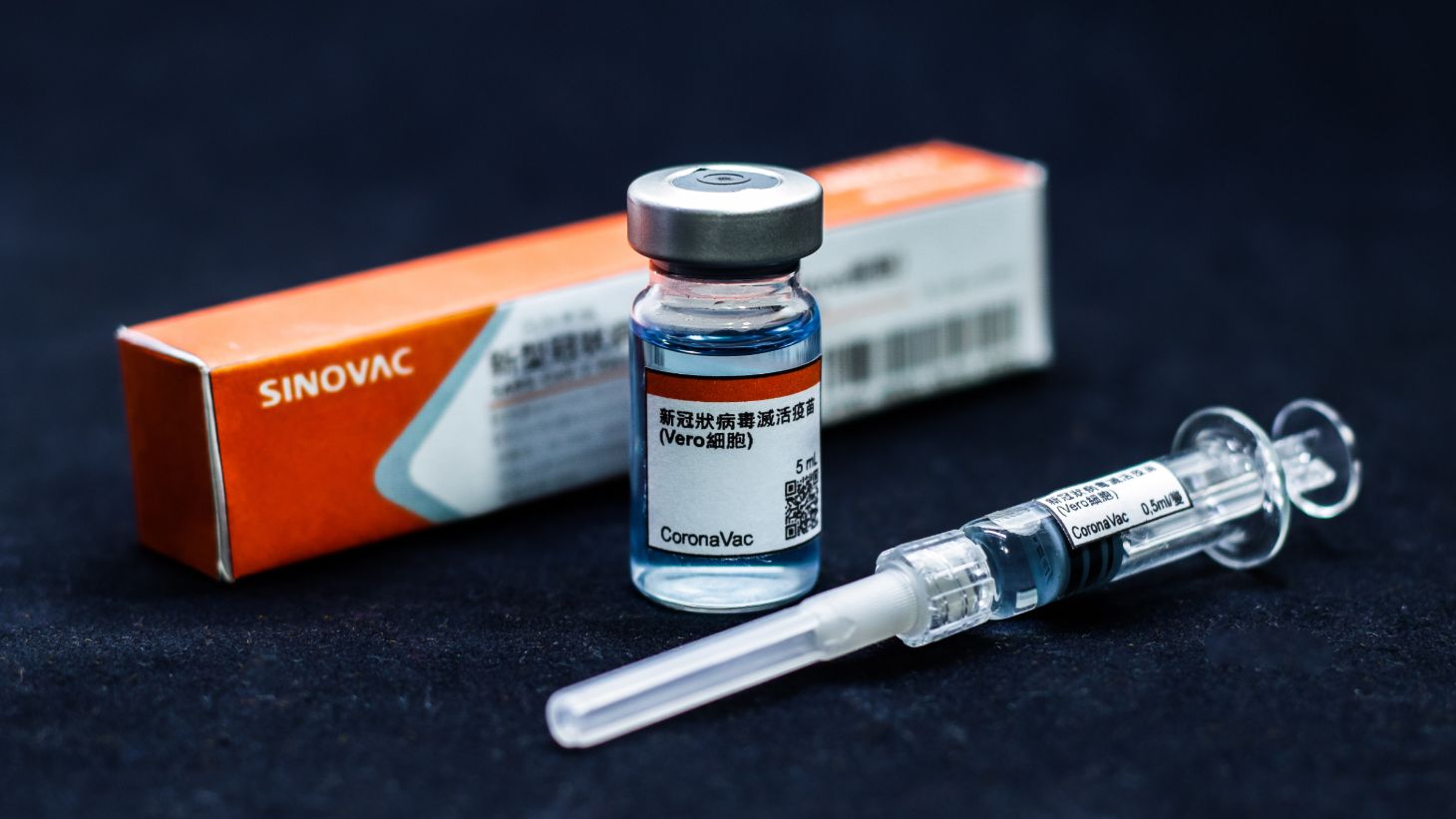
A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária (Anvisa) aprovou por unanimidade a autorização emergencial em caráter experimental do segundo lote da vacina CoronaVac, desenvolvida em parceria entre a farmacêutica chinesa Sinovac e o Instituto Butantan, ligado ao governo de São Paulo.
A diferença da análise do segundo lote para o primeiro está no fato de que o envase e os processos de rotulagem e embalagem ocorrem no Instituto Butantan. Essas 4,8 milhões de doses são produzidas na China pela farmacêutica Sinovac, que envia para esses procedimentos na sede do centro de pesquisa paulista.
Como a Anvisa já havia aprovado no último domingo (17) o primeiro lote importado da china, a avaliação da diretoria colegiada se deteve sobre as ações realizadas pelo Butantan.
A relatora, Meiruze Freitas, endossou os pareceres da área técnica e apresentou seu voto a favor da autorização, colocando alguns condicionantes sobre o acompanhamento de aplicação do imunizante para obter mais informações sobre sua estabilidade.
“Mesmo em cenário de incerteza, uma vacina contra a covid-19 segura, capaz de prevenir e reduzir mortalidade e morbidade, pode ser autorizada para o uso emergencial, em especial pelo contexto desta pandemia, onde há poucos tratamentos de suporte disponíveis e não há medicamentos registrados na Anvisa com indicações específicas para o tratamento da covid-19”, concluiu.
As incertezas mencionadas pela relatora dizem respeito a determinados resultados que não foi possível confirmar no processo de análise. É o caso do prazo de validade da eficácia das doses, já que não houve tempo ainda para aferir isso.
Leia Também
A área técnica entendeu que na impossibilidade de ter tais informações, é necessário que o Instituto Butantan mantenha o monitoramento e o envio de dados à Anvisa, especialmente caso ocorra algum problema. Mas considerou que o benefício é mais efetivo do que essas incertezas e apontou que diante da velocidade da vacinação dificilmente as doses do lote analisado passariam da validade, estimada em 12 meses.
O diretor Rômison Mota seguiu a relatora, manifestando sua posição favorável à autorização uma vez que é possível concluir que “benefícios conhecidos e potenciais superam seus riscos conhecidos e potenciais”. O diretor Alex Campos foi o segundo a seguir o voto da relatora, fazendo menção aos alertas quanto ao cumprimento de monitoramento para avaliar as incertezas apontadas no relatório.
A diretora Cristiane Gomes foi na mesma linha. O presidente da Agência, Antônio Barra Torres, concluiu a votação também acompanhando a posição da diretora Meiruze Freitas e fechando a aprovação por unanimidade.
Análise técnica
Antes dos diretores se manifestarem, representantes da área técnica explicaram o procedimento de análise e apresentaram seus pareceres. O gerente-geral de medicamentos e produtos biológicos, Gustavo Santos, ressaltou que o foco se deu no envase, rotulagem e embalagem realizados neste segundo lote nas instalações do Instituto Butantan.
Foram comparados doses fabricadas na condição original e na nova. Todos os documentos foram apresentados pelo Butantan. Os técnicos consideraram a relação benefício-risco da aplicação da vacina no contexto da pandemia. Mendes explicou o ponto da análise de estabilidade, que diz respeito à manutenção da eficácia da vacina durante o prazo de validade. Como não houve tempo suficiente para fazer este teste, foram considerados os parâmetros do primeiro lote.
“Entendemos que tendo em vista que procedimentos de vacinação não impactam de maneira significativa o desempenho da fabricação e que não acreditamos que possa haver impacto muito grande e sabemos que uso emergencial pressupõe uso rápido, a nossa argumentação foi no sentido de extrapolarmos o que foi determinado de estudo de estabilidade [do lote anterior] para este lote, o que equivale a 12 meses”, comentou.
Outra diferença entre primeiro e segundo lotes está nos frascos. Enquanto no primeiro era um frasco para cada dose, neste novo lote analisado cada frasco de 5 mililitros armazena 10 doses. Foi estimado que o tempo para uso do frasco é de oito horas para garantir a integridade do imunizante.
Por isso, será necessário cuidado para assegurar este prazo pelas equipes de saúde envolvidas na campanha de imunização. “A preocupação é que as técnicas assépticas sejam preservadas para que não haja qualquer risco de contaminação”, acrescentou Mendes
Pandemia completa 2 anos no Brasil com quase 650 mil mortes
Além das centenas de milhares de mortes, quase 30 milhões de brasileiros foram diagnosticados com covid-19 no período
Covid-19 volta a causar mais de mil mortes por dia no Brasil
Nas últimas semanas, Ministério da Saúde têm registrado sucessivamente novos recordes diários de casos da doença no Brasil
A alta estrutural do petróleo: como a questão ucraniana pode influenciar?
Tensões entre Ucrânia e Rússia podem pressionar os preços da commodity, dando uma mãozinha para o barril chegar à marca dos US$ 100
Covid-19 volta a ganhar força e Brasil bate recorde de casos confirmados da doença em 24 horas
Números de novos casos em apenas um dia ultrapassou a marca de 137 mil; Ministério da Saúde também confirmou mais 351 mortes pela doença
Com presidente do Conselho fura-quarentena e perdas de clientes, Credit Suisse tem desafio de recuperar reputação
Credit Suisse volta a ser abalado com saída de presidente do Conselho que veio para recuperar a imagem do banco, mas foi pego violando as regras da quarentena contra a covid-19
Ômicron e seus investimentos: variante do coronavírus terá efeitos distintos sobre empresas de saúde na bolsa; saiba quais são eles
Planos de saúde devem enfrentar um cenário menos favorável dado o aumento dos índices de sinistralidade e pressão sobre os custos
MacKenzie Scott, ex-mulher de fundador da Amazon, escolhe o Brasil para primeiro aporte em ONG fora dos EUA
O Vetor Brasil, organização que desenvolve profissionais para o setor público, receberá o dinheiro
Os yields devem estar loucos: entenda os impactos da alta dos juros nos EUA
2022 promete ser um ano no qual enfrentaremos o desconhecido. Não só pelos impactos da pandemia, mas também pela normalização monetária
Covid-19 volta a ameaçar planos de IPOs nos EUA
Ofertas públicas são adiadas por conta da variante Ômicron da covid-19
Depois da Azul, Latam cancela voos por casos de covid e gripe entre tripulantes
Diante dos problemas, Anac oferece suporte a passageiros afetados e monitora os casos entre profissionais da aviação
Vem aí a deltacron: Pesquisador afirma ter descoberto variante do coronavírus que mescla ômicron e delta
Autor da descoberta diz que ainda é cedo para antecipar os possíveis impactos da cepa; 25 casos foram confirmados até agora
Esquenta dos mercados: Bolsas operam mistas antes do payroll dos EUA e paralisação dos auditores da Receita pressiona governo federal
O Ibovespa ainda registra queda na casa dos 3% e o exterior morno não deve ajudar o índice brasileiro
Esquenta dos mercados: Bolsas e bitcoin (BTC) caem após ata do Fed, e Ibovespa deve aprofundar queda com risco fiscal do cenário doméstico
Os índices dos Estados Unidos tiveram uma queda expressiva ontem (05) após a divulgação do documento, e o Ibovespa, que já ia mal, piorou ainda mais
Esquenta dos mercados: Bolsas operam com cautela no exterior antes da ata do Fed e cenário doméstico permanece atento ao risco fiscal; ações de tecnologia caem lá fora após cerco da China contra setor
O coronavírus se espalha pelos países, que batem recordes de casos registrados nas últimas 24h e situação pode comprometer a retomada das atividades
Esquenta dos mercados: Bolsas do exterior sobem após dados positivos e Ibovespa deve destoar com cenário doméstico focado no risco fiscal mais uma vez
Além disso, a variante ômicron permanece no radar dos investidores internacionais, com maiores informações sobre infecções e letalidade
Anvisa recomenda suspensão da temporada de cruzeiros; três navios na costa brasileira registraram casos de covid a bordo
Dois navios interromperam as atividades na última sexta-feira, e o terceiro realizou o desembarque hoje, no Porto do Rio
Show da virada: bolsas americanas deixam Ibovespa no chinelo e encerram 2021 com ganhos de até 27%
Índices em Nova York sentem efeito do baixo volume do último dia do ano e fecham sessão abaixo dos recordes recentes. Temores por disparada de casos de covid-19 nos Estados Unidos também pesam.
Esquenta dos mercados: alerta da OMS sobre ômicron e delta atrapalha rali de final de ano nas principais bolsas mundiais
A organização alertou que a circulação simultânea das duas variantes pode provocar um tsunami de casos de covid-19
Em mais um dia fraco, Ibovespa perde força e fecha em queda; dólar volta a flertar com os R$ 5,70
Temores com a ômicron no exterior e volumes reduzidos limitaram novas altas, o que pesou na bolsa brasileira; juros e dólar responderam mal ao IGP-M e à pressão dos servidores públicos por aumentos
OMS alerta para tsunami de casos de covid-19 no mundo e manda recado ao Brasil; saiba o que a agência falou
Dois anos após primeiras notificações da China, circulação simultânea das variantes Delta e Ômicron provoca disparada global de infecções




























 SIGA O SD NO WHATSAPP
SIGA O SD NO WHATSAPP